Хроническая СН – комплексный полиэтиологичный клинический синдром, обусловленный первичным снижением насосной функции сердца, приводящий к сложным компенсаторным и патологическим реакциям гемодинамических, нейрогуморальных систем и к метаболическим нарушениям, что клинически проявляется одышкой, сердцебиением, повышенной утомляемостью, ограничением физической активности и признаками задержки жидкости в организме [1].
К сожалению, это лишь одна из немногих теоретических позиций, по которым существуют отечественные приоритеты в изучении ХСН. большинство современных диагностических и лечебных стратегий, известных нам из классических учебников и руководств по этой проблеме, требуют обновления на когортном и популяционном уровнях. Кроме того, для развития теории и клинической практики по проблеме хронической сердечной несостоятельности необходимы новые лабораторные и инструментальные уровни диагностики. К сожалению, указанные оптимальные условия для дальнейшего прогресса по обсуждаемому вопросу первично присутствуют в зарубежных странах, что предопределяет первичность получения новых теоретических и практических данных по клинике, диагностике и лечению ХСН в Европе и США и неизбежную ориентацию отечественной кардиологии на эти догматы. Тем не менее тщательный анализ и адаптация новых положений по СН, преломление предлагаемых данных на отечественную популяцию пациентов остается задачей российских кардиологов. Это утверждение убедительно подтверждает новый пересмотр отечественных рекомендаций по диагностике и лечению ХСН, обсуждавшийся активно в 2009 году и принятый ОССН к исполнению в 2010 году. Проанализировав указанный документ, а также предсуществующие рекомендации Американской коллегии кардиологов и Европейского общества кардиологов, мы можем с уверенностью сказать, что необходимая адаптация уже существует. В то же время целый ряд позиций, как нам кажется, требуют рассмотрения именно в оригинальном изложении. Для основы обзора по этой проблемы мы сочли необходимым ссылаться прежде всего на европейские источники, как более взвешенные и проверенные временем. В то же время многие американские положения блещут своей новизной и некоторой инвазивностью.
Таким образом, поскольку отечественные рекомендации по диагностике и лечению ХСН полностью соответствуют европейским от 2008 года, мы сочли возможным взять по следние за основу и отдельными ремарками характеризовать отечественные позиции по проблеме.
Несмотря на, казалось бы, четкие субъективные проявления заболевания верификация сердечной несостоятельности существенно запаздывает по отношению к изменениям гемодинамики. В этой связи отечественные и зарубежные исследователи стремятся развить направление донозологической диагностики ХСН, ведут поиск ранних маркеров СН.
В настоящей статье представлены новые лабораторные и инструментальные диагностические признаки, изложенные согласно рекомендациям Европейского – ESC (2008) и Американского – ACC / AHA (2009) обществ кардиологов, которые в дополнение к объективному обследованию помогают достоверно определить наличие ХСН.
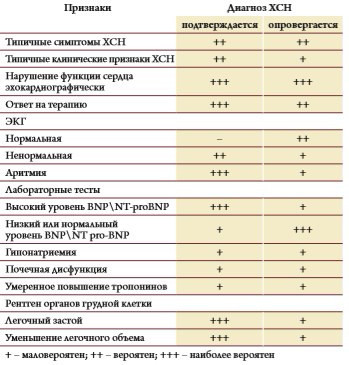
В таблице 1 представлена интегральная информация о диагностических подходах, рекомендуемых ведущими зарубежными кардиологическими обществами [2, 3]. рассматривая перечисленные в таблице 1 данные, имеющие основой результаты метаанализа множественных когортных исследований по ХСН, проведенного учеными бирмингемского университета Великобритании, можно сделать новые практические выводы. Например, такой симптом, как одышка, имеет высокую чувствительность (89 %), но низкую специфичность (51 %) и, следовательно, не может достоверно указывать на наличие или отсутствие ХСН. Клинические признаки с относительно высокой специфичностью включают: ИМ (89 %), ортопноэ (89 %), отеки (72 %), повышение давления в яремной вене (70 %), кардиомегалию (85 %), шумы в сердце (99 %), хрипы в легких (81 %) и гепатомегалию (97 %). Однако чувствительность этих признаков очень низкая, ее уровень колеблется в пределах от 11 % (шумы в сердце) до 53 % (отеки). Электрокардиография, уровень мозгового натрийуретического пептида (BNP), уровень Nконцевого пропептида (NTproBNP) имеют высокую чувствительность (89, 93 и 93 % соответственно). рентгенография органов грудной клетки умеренно специфична (76–83 %), но ее чувствительность составляет 67–68 %. По мнению J. Mant с соавт. (2009), уровень BNP более точно, чем ЭКГ, отражает наличие ХСН [4]. В диагностической точности не было выявлено различий между BNP и NTproBNP. Отечественные рекомендации по диагностике и лечению ХСН от 2009–2010 гг. приводят аналогичные позиции по обсуждаемой выше ассоциации признаков.
Таблица 1. Диагностические признаки, определяющие наличие ХСН.
По приведенным данным, можно заключить, что вероятность наличия ХСН целесообразно определять совокупностью признаков – и не только объективных, но прежде всего лабораторных и инструментальных. Согласно ESC Guide HF (2008) и ACC / AHA (2009) I класс рекомендаций для диагностики ХСН содержит многочисленные инструментальные подходы: регистрация ЭКГ (табл. 2); рентгенография органов грудной клетки (табл. 3); ЭхоКГ с определением ФВ, параметров сократимости миокарда ЛЖ и состояния клапанных структур (табл. 4); радионуклидные методы для определения ФВ ЛЖ; коронароангиография у пациентов с наличием стенокардии. Такие диагностические методы, как сбор анамнеза (выяснение Фр); объективное обследование; клинический анализ крови и мочи; биохимические маркеры крови, определяющие риск развития ССз (липидный профиль, глюкоза крови), функцию печени и почек, тиреоидный профиль (табл. 5), также имеют I класс рекомендаций [2, 3, 5, 6].
Таблица 2. Общие нарушения, выявляемые на ЭКГ у пациентов с ХСН.
Таблица 3. Нарушения, выявляемые на рентгенограммах органов грудной клетки у пациентов с ХСН.
Таблица 4. Эхокардиографические признаки ХСН.
Таблица 5. Общие нарушения лабораторных анализов, выявляемые у пациентов с ХСН.
На основании данных, приведенных в таблице 2, можно сделать заключение о полиморфности и незначительной специфичности ЭКГ изменений при ХСН [3], что, в свою очередь, затрудняет постановку окончательного диагноза без наличия высокоспецифичных признаков. регистрация ЭКГ, как диагностического показателя ХСН, рекомендована ACC / AHA (2009), как класс I (уровень доказательности С).
Отечественные рекомендации по диагностике и лечению ХСН 2009–2010 гг. в обсуждаемой совокупности признаков имеют практически полное соответствие.
Как и другие вышеуказанные признаки, рентгенологические нарушения имеют невысокую специфичность и чувствительность в диагностике ХСН [3]. В этой связи использование рентгенологического исследования органов грудной
клетки в диагностике ХСН применяется реже, в то время как употребление более специфичного и чувствительного теста на определение уровня BNP и NTproBNP заметно увеличилось в последние годы. Кроме того, значительные преимущества в диагностике и лечении ХСН при использовании тестов на BNP и NTproBNP показаны во многих клиниче ских исследованиях. В свою очередь, это привело к включению тестов на BNP и NTproBNP в рекомендации по диагностике ХСН Европейской и Американской ассоциациями кардиологов и широкому распространению этих тестов в современной клинической практике.
Лабораторные показатели, приведенные в таблице 5, косвенно указывают на наличие ХСН, а наибольшей специфичностью и чувствительностью обладает тест на BNP и NTproBNP [3]. Повышенный уровень NTproBNP и BNP, по данным многих зарубежных и отечественных работ, четко ассоциирован с наличием избыточного напряжения стенок миокарда, возникающего при инициации и усугубляющегося при прогрессировании и декомпенсации ХСН. результаты работы французских ученых показывают, что пациенты со сниженным уровнем BNP в процессе лечения по факту острой декомпенсации ХСН имели значительно более низкий уровень смертно сти на 30 и 180й день по сравнению с пациентами, у которых отмечено незначительное повышение или неизменные уровни BNP [7]. Исходя из результатов вышеуказанного эталонного исследования уровень BNP является подходящим прогностическим фактором для определения риска смертности у больных СН.
Анализ отечественной литературы и практической дея тельности стационаров и поликлиник города СанктПетербурга по вопросам применения обсуждаемых методов лабораторной диагностики показал, что несмотря на наличие в отечественных рекомендациях ОССН аналогичных позиций, практическое рутинное применение оценки уровней альбумина, тропонинов, натрия осуществляется лишь в некоторых отделениях интенсивной терапии и вовсе не используется в поликлинических или стационарных подразделениях.
В университете Медицинского центра Nebraska и технологическом НьюЙоркском университете было проведено обследование больных ХСН ишемического и неишемического генеза. результаты данного исследования также свидетельствуют о возможности использования уровня BNP плазмы крови для определения глобальной функциональной мощности и объема специфической нагрузки на миокард у пациентов без наличия интенсивных физических нагрузок [8]. По данным ученых, уровень NTproBNP и BNP возрастает пропорционально ремоделированию миокарда. В многоцентровом исследовании Breathing Not Properly (BNP) были обследованы 1586 пациентов с высокоинтенсивной одышкой на момент поступления в ОрИТ. В перечень обследования включался анализ крови на BNP. В результате анализа выявлена зависимость между степенью миокардиального стресса и уровнем BNP [9, 10]. В канадском исследовании IMPROVE–CHF был обследован 501 больной. Согласно полученным результатам выявлено 25 %е снижение затрат на лечение и обследование пациентов, которым проводился анализ уровня BNP, по сравнению с группой, в которой не использовалось определение уровня BNP [11, 12]. Сходные данные были получены и в исследовании BASEL [13]. Имеются данные об эффективности оценки уровня BNP у пациентов с одышкой для дифференциальной диагностики заболеваний легких и наличия ХСН [14]. В исследование, проведенное учеными университета Мальмо (г. Лунд, Швеция) у пациентов с АГ при нарастании уровня маркеров ремоделирования миокарда нарастал уровень BNP [15]. Исходя из вышесказанного, BNP может быть использован, как скрининговый показатель для наиболее быстрой и точной верификации наличия ХСН у пациентов с отеками и одышкой, и может служить скрининговым показателем для отбора на дальнейшее ультразвуковое исследование сердца, что позволяет существенно сократить время на обследование больных ХСН и другими патологиями со сходными симптомами.
Эхокардиография является общепринятым методом для определения жизнеспособности и сократительной функции миокарда, но оценка данных этого метода очень субъективна. В таблице 4 указаны ЭхоКГ параметры, которые согласно ESC 2008 рекомендовано использовать для диагностики ХСН. Высокоспецифичными ЭхоКГ признаками являются: ФВ ЛЖ, конечный систолический и конечный диастолический объемы, фракция укорочения, временной интеграл скорости в тракте оттока ЛЖ. Остальные параметры, приведенные в таблице 4, также используются в комплексном исследовании сердца при обследовании больного ХСН.
Несмотря на широкое внедрение ЭхоКГ в отечественную кардиологическую практику, лишь немногие протоколы содержат ссылки на ассоциацию ХСН и конечного систолического размера ЛЖ. Также очень низок уровень использования интеграла скоростьвремя (VTI) в тракте оттока ЛЖ.
Наиболее чувствительными и специфичными для верификации сердечной несостоятельности являются допплерографические показатели, представленные в таблице 6 [3]. Параметры, получаемые в режиме тканевой допплерографии, на данный момент недостаточно изучены и в рекомендации ESC2008 по диагностике ХСН внесены как класс IIa, уровень доказательности С. Тем не менее они позволяют заподозрить ХСН на наиболее ранних, доклинических стадиях развития (стадия A по номенклатуре Американской ассоциации кардиологов). Эти параметры играют важную роль в стратификации риска и определении прогноза течения ХСН [6].
Таблица 6. Допплерэхокардиографические признаки ХСН.
Отечественные рекомендации ОССН содержат все обсуждаемые допплерографические индексы, однако, к сожалению, уровни рекомендуемости не соответствуют возможностям их практического применения.
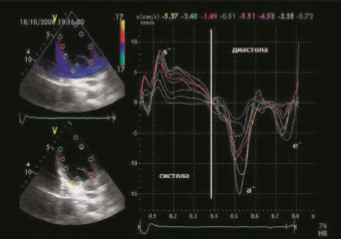
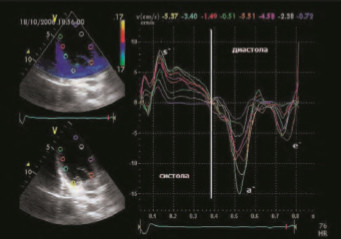
Проведение ЭхоКГ в режиме тканевой скоростной визуализации – Tissue Velocity Imaging (TVI) – с последующим количественным анализом (Qанализом) позволяет в цифровом выражении оценить глобальную и локальную сократимость, определив скорость движения сегментов миокарда в систолу (s`) и диастолу (e` и a` пики), как показано на рисунке 4 [16, 17]. Это исследование возможно выполнить на ультразвуковом аппарате фирмы GE vivid 7 (США).
Рисунок 4. Qанализ волновой формы TVI.
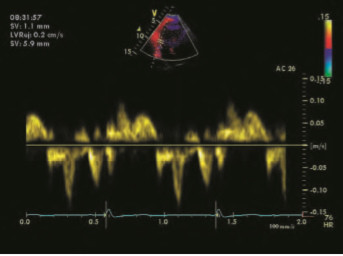
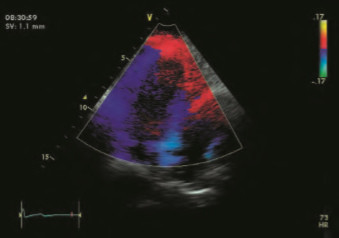
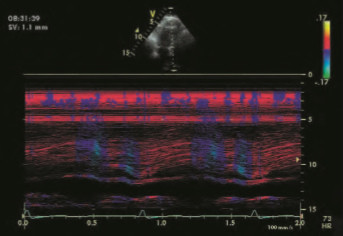
TVI – это методика, в которой используется регистрация смещения частоты допплеровского спектра для количественной оценки движения миокарда. Методика TVI может использоваться, чтобы оценить глобальную и региональную систолическую и диастолическую функции миокарда. Преимущество методики TVI заключается в том, что регистрируется смещение частоты допплеровского спектра отраженного сигнала. Это дает клиницистам возможность оценки функции миокарда даже в том случае, когда качество двухмерного изображения может быть не оптимальным. Как и в режиме обычного допплеровского картирования, режим TVI может отображаться, как импульсноволновой допплер (рис. 1), цветовой допплер (рис. 2), цветовой допплер в режиме M–Mode (рис. 3), TVI в волновой форме с возможностью оценки в режиме Qанализа (рис. 4) [ 17–20].
Рисунок 1. Импульсноволновой TVI.
Рисунок 2. Цветовой TVI.
Рисунок 3. TVI M-Mode.
Рисунок 4. Qанализ волновой формы TVI.
Изучению тканевых характеристик допплеровского плана у больных ХСН посвящены многие современные работы. Так, тегеранскими учеными было проведено исследование лонгитудинальной сократимости миокарда ЛЖ в режиме тканевой допплерЭхоКГ. В этом исследовании определялась скорость движения миокарда при лонгитудинальном сокращении у больных с наличием акинетичных (нежизнеспособных) и нормальных (жизнеспособных) нижнебазальных сегментов миокарда ЛЖ. Определялся и эффект добутамина на движение нежизнеспособных сегментов миокарда. В рамках исследования проанализированы 2 группы: 25 пациентов (мужчины в возрасте 59±7,69 лет) с наличием акинетичных сегментов (группа наблюдения) и 14 пациентов (мужчины в возрасте 56±11,90 лет) без признаков поражения коронарных сосудов с нормальными результатами ЭхоКГ (контрольная группа). У всех пациентов регистрировались следующие параметры TVI: скорость движения миокарда в фазу изгнания (Sm, см / c) и пиковая систолическая деформация (ST, %). В результате было отмечено значительное снижение скорости движения миокарда в фазу изгнания у группы больных с акинетичными (нежизнеспособными) сегментами по отношению к контрольной группе пациентов (3,58±1,08 см / c против 5,56±1,28 см / c; р<0,001), а также значительное снижение интервала ST (–3,86 %±4,12 % против –17,64 %±7,44 % соответственно, р<0,001). В заключение было показано снижение всех параметров TVI у пациентов с акинетичными (нежизнеспособными) сегментами миокарда ЛЖ по сравнению с пациентами без признаков поражения коронарных сосудов. Это говорит о диагностической значимости проведения ЭхоКГ исследования в режиме TVI и возможности оценки параметров не субъективно, а в объективном количественном формате [21, 22].
В следующем исследовании проводилась оценка ответа миокарда на физическую нагрузку при проведении велоэргометрического стресс теста в положении лежа и в положении сидя у здоровых мужчин. В ходе исследования определялись следующие скоростные параметры: скорость миокарда во время изоволюмического сокращения (isovolumic contraction velocity – IVCV), пиковая скорость во время систолы (peak systolic velocity – PSV), скорость изоволюмического расслабления (isovolumic relaxation velocity – IVRV), раннего диастолического расслабления (peak early diastolic velocity – e') и позд него диастолического расслабления (peak late diastolic velo city – a'). В результате были получены незначительные различия между тестами в определяемой PSV. Наоборот, при регистрации e' результат значительно больше различался (р<0,001), при нагрузке в положении лежа IVRV была снижена более существенно (р<0,001). Исходя из полученных в этом исследовании данных, можно судить о возможности количест венной оценки сократимости миокарда ЛЖ при использовании методики TVI не только в покое, но и при проведении стресстеста [23]. В Копенгагенском исследовании (the Copenhagen City Heart Study) обследовано 1 036 пациентов, которым было проведено как стандартное ЭхоКГ исследование, так и в режиме тканевого допплера с последующим Qанализом [15]. В исследовании проводили регистрацию пиковой скорости и лонгитудинального смещения движения миокарда в систолу (s`), раннюю диастолу (е`), позднюю диастолу (a`), а также определяли соотношение E и e` пиков (E / e`). В исследование были включены 345 человек с АГ, 65 больных СД и 93 больных ИбС. Контрольная группа – 533 здоровых человека. Всего у 11 (1,07 %) больных отмечалось снижение ФВ ЛЖ менее 50 %. По результатам исследования, при оценке вышеупомянутых тканевых параметров движения стенок было выявлено снижение как систолической, так и диастолической функции миокарда ЛЖ, что говорит о высокой чувствительности этого метода и возможности использования его на ранних стадиях ХСН. В исследованиях, проводимых в ведущих университетах и кардиологических клиниках мира, показана связь нарушений систолической и диастолической функций миокарда ЛЖ с такими поражениями миокарда, как амилоидное, гипертрофическая кардиомиопатия и многие другие [24, 25].
Таким образом, внедрение в перечень диагностических критериев ХСН показателей глобальной лонгитудинальной сократимости миокарда ЛЖ и других параметров тканевого допплеровского исследования представляется весьма перспективным (табл. 6).
В исследовании PROBE–HF были исследованы 1 012 человек с наличием АГ и / или СД без наличия симптомов и признаков ХСН. Всем исследуемым проводилось ЭхоКГ исследование для определения асимптоматической левожелудочковой дисфункции и анализ уровня BNP. По результатам исследования, уровень BNP был повышен во всех группах, как с систолической, так и диастолической левожелудочковой дисфункцией. Исходя из этих результатов эксперты Европейского и Американского кардиологических обществ рекомендуют проводить анализ уровня BNP у всех больных АГ и диабетом для определения бессимптомной левожелудочковой дисфункции перед проведением ЭхоКГ [26].
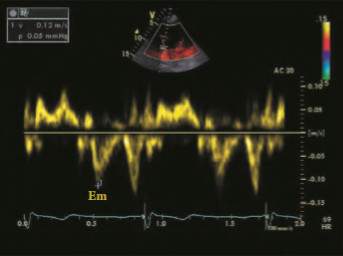
Российскими учеными, членами Всероссийского национального общества кардиологов (ВНОК) к параметрам диагностики ХСН на 2010 год отнесены симптомы и объективные признаки, ЭКГ, гематологические и биохимические анализы крови, общий анализ мочи, ЭхоКГ, магнитнорезонансная томография, радиоизотопные методы, рентгенография органов грудной клетки [27]. Анализ уровней BNP и NTproBNP в российских рекомендациях не входит в перечень стандартных биохимических анализов, рекомендуемых для диагностики ХСН. Описывается высокая чувствительность и специфичность методов для исключения наличия ХСН, а также возможность использовать их для оценки долгосрочного прогноза. В рамках ЭхоКГ исследования для определения стадий диастолической дисфункции рекомендуется использование некоторых допплерЭхоКГ признаков, указанных в таблице 6, а также определение Em методом тканевой допплерЭхоКГ (рис. 5), что отражает скорость движения митрального клапана в раннюю диастолу.
Рисунок 5. Тканевая доплерография.
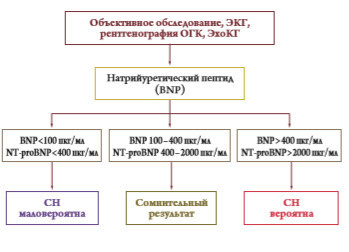
Исходя из вышепредставленных данных и принимая в рассмотрение наиболее специфичные и чувствительные методики скрининга сердечной несостоятельности, можно сформировать алгоритм диагностики ХСН в виде нижеприведенной блоксхемы (рис. 6).
Рисунок 6. Алгоритм диагностики ХСН (ESC, 2008).
Подводя итог изложению современных методов диагностики СН, хотелось бы отметить, что ХСН манифестирует комплексом клинических синдромов, содержащих как низкоспецифичные, так и малочувствительные признаки и симптомы. Среди лабораторных маркеров BNP является наиболее привлекательным благодаря своим уникальным патофизиологическим ассоциациям: раннее выделение в плазму крови
при минимальной перегрузке ЛЖ давлением или объемом. В литературе имеются убедительные данные надежности использования BNP в качестве маркера наличия или отсутствия ХСН. роль BNP, как предиктора уровня риска осложнений у пациентов с тяжелой ХСН, после перенесенного ИМ еще не до конца изучена, и исследования, посвященные этой проблематике, еще не закончены. Весьма перспективным маркером ранних стадий ХСН представляется методика TVI, которая дает возможность количественно оценивать не только глобальную, но и локальную сократительную функцию миокарда ЛЖ.
В заключение можно отметить, что на современном этапе заподозрить наличие ХСН можно на основании неспецифичных субъективных и объективных симптомов, а уточнить факт СН необходимо по скрининговым тестам (BNP, NTproBNP) и только затем проводить углубленное исследование, нацеленное на выявление всех гемодинамических, этиологических и патогенетических нарушений у пациента для определения наиболее эффективной тактики ведения.
Список литературы:
1. Обрезан А. Г., Вологдина И. В. Хроническая сердечная недостаточность.–СПб: «Вита Нова». – 2002. – 320 с.
2. Jessup M, Abraham WT, Casey DE et al. 2009 focused update: ACCF / AHA
Guidelines for the Diagnosis and Management of Heart Failure in Adults: a report of the American College of Cardiology Foundation / American Heart Association Task Force on Practice Guidelines: developed in collaboration with the International Society for Heart and Lung Transplantation. Circulation. 2009;119 (14):1977–2016.
3. Dickstein K, CohenSolal A, Filippatos G et al. ESC Guidelines for
the diagnosis and treatment of acute and chronic heart failure 2008: the Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure 2008 of the European Society of Cardiology. Developed in collaboration with the Heart Failure Association of the ESC (HFA) and endorsed by the European Society of Intensive Care Medicine (ESICM). Eur Heart J. 2008;29 (19):2388–2442.
4. Mant J, Doust J, Roalfe A et al. Systematic review and individual patient
data metaanalysis of diagnosis of heart failure, with modelling of implications of different diagnostic strategies in primary care. Health Technol Assess. 2009;13 (32):1–207.
5. Мошина В. А., Верткин А. Л., Сапрыгин Д. б. роль мозгового натрий уретического пептида в стратификации риска у больных с острым коронарным синдромом без подьема ST. Лабораторная медицина. 2005;7:95–102.
6. Напалков Д. А., Сеидова Н. М., Сулимов В. А. Хроническая сердечная
недостаточность: смещение фокуса на начальные стадии заболевания. Лечащий врач. 2008;4:58–60.
7. CohenSolal A, Logeart D, Huang B et al. Lowered Btype natriuretic peptide in response to levosimendan or dobutamine treatment is associated with improved survival in patients with severe acutely decompensated heart failure. J Am Coll Cardiol. 2009;53 (25):2349–2352.
8. Norman JF, Pozehl BJ, Duncan KA et al. Relationship of Resting Btype
Natriuretic Peptide Level to Cardiac Work and Total Physical Work Capacity in Heart Failure Patients. J Cardiopulm Rehabil Prev. 2009;29 (5):310–313.
9. Mueller C, Scholer A, LauleKilian K et al. Use of Btype natriuretic peptide in the evaluation and management of acute dyspnea. N Engl J Med. 2004;350 (7):647–654.
10. Newton PJ, Betihavas V, Macdonald P. The role of btype natriuretic peptide in heart failure management. Aust Crit Care. 2009;22 (3):117–123.
11. Greenberg B. Can we IMPROVECHF management by measuring natri
uretic peptides? Circulation. 2007;115 (24):3045–30457.
12. Moe GW, Howlett J, Januzzi JL, Zowall H. Nterminal proBtype natriuretic peptide testing improves the management of patients with suspected acute heart failure: primary results of the Canadian prospective randomized multicenter IMPROVECHF study. Circulation. 2007;115 (24):3103–3110.
13. Boldanova T, Noveanu M, Breidthardt T et al. Impact of history of heart
failure on diagnostic and prognostic value of BNP: Results from the B type Natriuretik Peptide for Acute Shortness of Breath Evaluation (BASEL) Study. Int J Cardiol. 2009 Jan 28. [Epub ahead of print].
14. Morrison LK, Harrison A, Krishnaswamy P et al. Utility of a rapid Bnatri
uretic peptide assay in differentiating congestive heart failure from lung disease in patients presenting with dyspnea. J Am Coll Cardiol. 2002;39 (2):202–209.
15. Magnusson M, Jovinge S, Rydberg E et al. Natriuretic peptides as indicators
of cardiac remodeling in hypertensive patients. Blood Press. 2009 Jun 26:1–8.
16. Rasmus Mogelvang, Peter Sogaard, Sune A. Pedersen et al. Tissue Doppler
echocardiography in persons with hypertension, diabetes, or ischaemic heart disease: the Сopenhagen City Heart Study European Heart Journal. 2009;30:731–739.
17. Andersen NH, Poulsen SH. Evaluation of the longitudinal contraction 17.
of the left ventricle in normal subjects by Doppler tissue tracking and strain rate. J Am Soc Echocardiogr. 2003;16 (7):716–723.
18. Pan C, Hoffmann R, Kuhl H et al. Tissue tracking allows rapid and accurate visual evaluation of left ventricular function. Eur J Echocardiogr. 2001;2 (3):197–202.
19. Sogaard P, Egeblad H, Kim WY et al. Tissue doppler imaging predicts
improved systolic performance and reversed left ventricular remodeling during longterm cardiac resynchronization therapy. J Am Coll Cardiol. 2002;40 (4):723–730.
20. Waggoner AD, Bierig SM. Tissue Doppler imaging: a useful echocardio
graphic method for the cardiac sonographer to assess systolic and diastolic ventricular function. J Am Soc Echocardiogr. 2001;14 (12):1143–1152
21. Sadeghian H, Majidi S, LotfiTokaldany M et al. Evaluation of longitudinal
tissue velocity and deformation imaging in akinetic nonviable inferobasal segments of left ventricular myocardium by dobutamine stress echocardiography. Echocardiography. 2009;26 (7):801–806.
22. Schneider C, Bahlmann E, Malisius R et al. Tissue velocity imaging during dobutamine stimulation for assessment of myocardial viability: segmental analysis in patients after myocardial infarction. Int J Cardiol. 2006;110 (1):15–21.
23. Bjallmark A, Larsson M, Shahgaldi K et al. Differences in myocardial velocities during supine and upright exercise stress echocardiography in healthy adults. Clin Physiol Funct Imaging. 2009;29 (3):216–223.
24. Bayrak, Fatih, Kahveci et al. Tissue Doppler imaging to predict clinical
course of patients with hypertrophic cardiomyopathy. Eur J Echocardiogr. 2008;9 (2):278–283.
25. Bellavia D, Pellikka PA, Abraham TP et al. Hypersynchronisation by tissue velocity imaging in patients with cardiac amyloidosis. Heart. 2009;95 (3):234–240.
26. Betti I, Castelli G, Barchielli A et al. The role of Nterminal PRO brain natriuretic peptide and echocardiography for screening asymptomatic left ventricular dysfunction in a population at high risk for heart failure. The PROBEHF study. J Card Fail. 2009;15 (5):377–384.
27. Оганов р. Г., Мамедов М. Н. Национальные клинические рекомендации ВНОК. – М.: «СилицеяПолиграф», 2008. – 512с.
Источник: Обрезан А.Г., Косарев М.М., Стрельников А.А. Клинические и лабораторные инструментальные маркеры диагностики ХСН // Журнал Сердечная Недостаточность. Том 11, № 3 (59), 2010 г. с. 177-184