Микрохирургическое удаление
В. Б. Семенютин, П. И. Никитин, В. А. Алиев, И. М. Бухаев, Г. К. Панунцев
В начале 80-х гг. XX в. были разработаны доплеровские приборы, предназначенные для нужд микрохирургии. Они отвечают основным требованиям, в частности позволяют проводить инсонацию сосудов диаметром менее 1 мм под визуальным контролем при непосредственном контакте датчика с сосудом в условиях узкой операционной раны; позволяют осуществлять раздельное исследование близко расположенных артерий. Этим требованиям отвечают импульсный доплеровский режим с высокой частотой излучения (16–20 МГц). Первый прототип такого прибора был создан P. Cathignol с соавт. в 1978 году.
Аппаратура позволяет регистрировать поток крови в любых сосудах, лежащих в непосредственной близости от миниатюрного датчика (диаметром от 1 до 3 мм), начиная от пиальных и перфорантных артерий и вен диаметром от 0,3 мм (рис. 9.1) и заканчивая артериями основания мозга диаметром до 4 мм. Чаще всего микрососудистая контактная доплерография (МСДГ) проводится с использованием контрольного объема 1–2 мм, что позволяет получить наиболее качественный спектр. Что касается угла наклона датчика, то соблюдение величин, рекомендованных для чрескожного озвучивания, чаще всего оказывается невозможным, в связи с чем необходимо стараться соблюдать постоянный угол при локации различных сосудов для получения сравнимых данных. Реальные величины угла не должны превышать 60°. При исследовании регистрируются стандартные параметры: средняя максимальная (огибающая) частота (скорость), средневзвешенная частота (скорость), систолическая частота (скорость), индексы периферического сопротивления. Основное внимание уделяется динамике этих показателей в процессе выполнения манипуляций.
Аспекты применения МСДГ в процессе удаления артериовенозных мальформаций головного мозга изучены недостаточно. В настоящее время доказанной является ценность метода в выявлении питающих артерий, особенно при глубоко расположенных мальформациях, когда визуально определить, является ли обнаруженная в глубине борозды артерия питающей или нет, весьма затруднительно. С другой стороны, МСДГ дренирующих вен мальформации позволяет определить момент, когда оказываются выключенными основные источники кровоснабжения шунта, особенно при фистульном типе АВМ.
Наконец, в связи с неразрешенностью вопроса о состоянии кровоснабжения здорового мозга, особенно в непосредственной близости от АВМ, МСДГ позволяет селективно оценивать реактивность в здоровых артериях путем изменения напряжения углекислого газа в крови. Исследования W. Hassler (1986) свидетельствуют в пользу сохранения реактивности в паранидальном сосудистом ложе в полном объеме, что, однако, требует подтверждения.
Использование современной микрохирургической техники для удаления АВМ, расположенных в «функционально значимых» зонах головного мозга, позволяет произвести полное удаление АВМ, тем самым свести к минимуму возможность повторных геморрагий из ее остатков (Muacevic A., Steiger H., 1999; Yamada S. et al., 1999; Pik J., Morgan M., 2000). Поэтому на первый план выдвигается проблема максимального сохранения мозговых структур, окружающих АВМ. Для решения этой проблемы предложены различные методы оценки функционального состояния этих структур (Maldjian J. et al., 1996; Nyberg G. et al., 1996; Stapleton S. et al., 1997; Vinas F. et al., 1997; Kato Y. et al., 1998; Duffau H. et al., 1999; Kombos T. et al., 1999; Mine S. et al., 1999; Seghier M. et al., 2001) и кровотока в сосудах АВМ и окружающих их структур головного мозга (Hassler W., Gilsbach J., 1984; Hassler W., 1986; Black K. et al., 1988; Rubin J. et al., 1989; Pietila T. et al., 1998; Schaller C. et al., 1998; Zamorano L. et al., 1998).
Для интраоперационной идентификации АВМ наиболее часто используются системы дуплексного сканирования для получения их изображения, позволяющие выявить AВМ и с высокой точностью обеспечить безопасную навигацию. Методика также позволяет выявлять афферентные и эфферентные сосуды АВМ (Rubin J. et al., 1989; Black K. et al., 1998; Woydt M. et al., 1998; Otsuki H. et al., 2001; Woydt M. et al., 2001). При этом некоторые авторы подчеркивают и возможность интраоперационного подтверждения удаления АВМ (Rubin J. et al., 1989; Black K. et al., 1998; Woydt M. et al., 1998). В то же время недостатки, связанные с невозможностью идентификации сосудов диаметром меньше 1 мм или большего диаметра, но расположенных поверхностно, не позволяют оценить кровоток в афферентных и эфферентных сосудах небольших по объему АВМ, расположенных в «функционально значимых» зонах головного мозга и транзитных артерий, проходящих по поверхности мозга в глубине борозд (Woydt M. et al., 1998).
Использование МСДГ по методу W. Hassler (1986) и оригинального приспособления, представленного на рис. 9.1, позволяющего изменять угол между осью датчика и исследуемым сосудом, а также фиксировать торец датчика на его стенке, позволяет идентифицировать афферентные, эфферентные и транзитные сосуды на основании полученных данных ЛСК и ПИ практически независимо от их расположения и диаметра. В то же время в некоторых случаях, особенно при расположении афферентных и дренирующих сосудов на большой глубине, не всегда удается получить необходимые данные, хотя это и не сказывается на результатах оперативного вмешательства. Подключение в этом случае дуплексного сканирования было полезным и позволило уменьшить неопределенность при удалении таких АВМ.
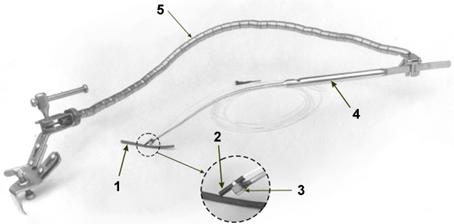
Рис. 9.1. Устройство для контактной МСДГ, обеспечивающее автоматическую фиксацию датчика в оптимальном положении на исследуемом сосуде и позволяющее проводить длительный мониторинг ЛСК, не прерывая хирургических манипуляций: 1 – исследуемый сосуд, 2 – 20 МГц датчик, 3 – миниатюрный зажим, 4 – направляющее устройство, 5 – ретрактор (Говоров Б. Б. с соавт., 2004)
Афферентные и эфферетные сосуды АВМ не всегда могут быть визуально идентифицированы: и тем и другим артериальная кровь придает одинаковый бордово-красный цвет, диаметр их, как правило, примерно равный, а параллельный ход сосудов часто еще более затрудняет распознавание. Наиболее затруднительной представляется визуальная диагностика транзитных сосудов. Такие сосуды также располагаются в мозговых бороздах, часто имеют идентичный цвет и диаметр. Направляясь к клубку АВМ и симулируя афферентный сосуд, транзитный сосуд может резко изменить свое направление и направиться в глубину мозгового вещества, не принимая участие в кровоснабжении мальформации.
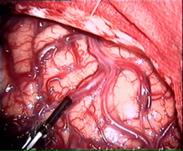
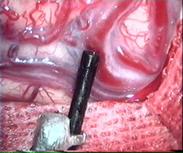
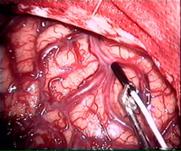
На рис. 9.2 представлены МСДГ-паттерны в афферентном, эфферентном и транзитном сосудах, зарегистрированные у больной перед удалением поверхностной АВМ, расположенной в «функционально значимой» зоне головного мозга.
РИСУНКИ СТРОГО НИЖНИЕ ПОД ВЕРХНИМИ! Расположить оба на одной полосе!
|
|
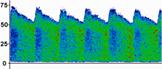

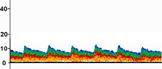
Рис. 9.2. Интраоперационный вид и спектры ЛСК до удаления АВМ затылочной доли у больной 35 лет. Слева направо афферентный, эфферентный сосуды, транзитная артерия (Семенютин В. Б. с соавт., 2001)
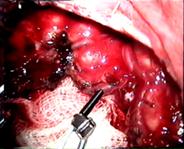
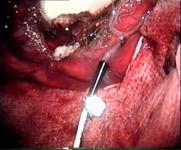
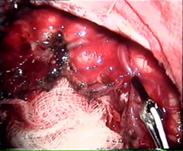
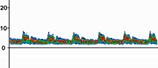

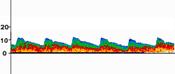
Рис. 9.3. Интраоперационный вид и спектры ЛСК после удаления АВМ затылочной доли у больной 35 лет. Обозначения те же, что и на рис. 9.2 (Семенютин В. Б. с соавт., 2001)
После удаления АВМ (полнота удаления контролируется по исчезновению артериального компонента во всех дренирующих сосудах) кровоток в сосудах, частично питающих АВМ, должен существенно снижаться до величин, зарегистрированных в транзитных сосудах до удаления АВМ, что наряду с сохранением проходимости транзитных артерий крайне важно для сохранения нормальной перфузии церебральных структур (рис. 9.3).
В настоящее время показана целесообразность использования комбинации методов МСДГ и дуплексного сканирования для проведения интраоперационного мониторинга при удалении АВМ, расположенных в различных (не только поверхностных) «функционально значимых» зонах головного мозга. Отличие кинетических и спектральных характеристик ЛСК в афферентных, эфферентных и транзитных сосудах АВМ при МСДГ-мониторинге позволяет проводить их идентифицикацию. Метод МСДГ позволяет в динамике (на различных этапах операции) оценивать кровоток в афферентных, эфферентных и транзитных сосудах в поверхностных АВМ, расположенных в «функционально значимых» зонах головного мозга. Оценка показателей, полученных при МСДГ афферентных и эфферентных сосудов, позволяет контролировать полноту удаления АВМ. Сохранение кровотока в транзитных сосудах поверхностных АВМ, расположенных в «функционально значимых» зонах головного мозга, позволяет избежать дополнительной инвалидизации больных после радикальных операций.
Следующая глава:
Эмболизация и функциональное значение афферентных сосудов
Предыдущая глава:
Литература
